2Sanatorio Antártida. Buenos Aires, Argentina.
RESUMEN
Introducción: la artritis séptica (AS) asociada a la cirugía de reconstrucción del ligamento cruzado anterior (RLCA) es una complicación infrecuente, pero potencialmente devastadora. La incidencia oscila entre 0.14 y 1.8 %. Existe abundante bibliografía que sostiene que la utilización de vancomicina para embeber los injertos de semitendinoso y recto interno (ST-RI) puede generar una reducción del riesgo de infección, pero es escasa la literatura en la que se demuestre el costo-beneficio económico que tiene la implementación sistemática de este protocolo.
Objetivos: evaluar si es costo-efectivo conveniente el uso de vancomicina como coadyuvante para prevenir la AS en la RLCA primaria. En forma secundaria se reportaron resultados funcionales y complicaciones del procedimiento.
Materiales y métodos: se realizó un estudio prospectivo, ciego y randomizado, desde febrero de 2020 hasta febrero de 2023. Se reclutaron 250 pacientes con RLCA con ST-RI cuádruples. Un grupo de intervención con injertos embebidos con vancomicina y el grupo de control sin antibiótico. Seguimiento mínimo de 2 años.
Resultados: en el grupo A (con vancomicina), de 122 pacientes, no se reportaron infecciones. En el grupo B (sin vancomicina), de 123 pacientes, hubo 3 infecciones (p = 0.247). En el grupo A se gastaron 427 dólares ($3.5 por ampolla de vancomicina); mientras que en el grupo B, debido a los 3 casos de infecciones, se gastaron 4254 dólares. No se registraron diferencias en relación al tiempo quirúrgico y dolor postoperatorio. Los pacientes del grupo A manifestaron mayor satisfacción. Sin diferencias significativas entre ambos grupos en relación a resultados funcionales y a complicaciones no infecciosas como artrofibrosis y rerrotura.
Conclusiones: el estudio muestra que, en el contexto de una RLCA primaria con injertos de ST-RI, el uso de vancomicina tópica disminuye la incidencia de AS y, en consecuencia, los gastos excesivos asociados a su tratamiento, por lo que resulta una valiosa estrategia costo-efectiva. No altera en forma significativa los resultados funcionales, la cicatrización del injerto ni las complicaciones no infecciosas asociadas.
Palabras clave: Artritis séptica; Vancomicina en RLCA; Costo-beneficio; Complicaciones
Nivel de evidencia: II. Estudio de Cohorte Prospectivo
Vancomycin in Primary Anterior Cruciate Ligament Reconstruction. Is it Cost-Effective?
ABSTRACT
Introduction: septic arthritis (SA) associated with anterior cruciate ligament reconstruction surgery (ACLR) is a rare but potentially devastating complication. The incidence ranges between 0.14 and 1.8%. There is abundant literature that maintains that the use of vancomycin to soak STRI grafts can reduce the risk of infection, but there is little literature that demonstrates the economic cost-benefit of the systematic implementation of this protocol.
Objectives: to evaluate whether it is cost-effective to use vancomycin as an adjuvant to prevent AS in primary RLCA. Secondary functional results and complications of the procedure were reported.
Materials and methods: a prospective, blinded and randomized study was carried out, from February 2020 to February 2023. Two hundred and fifty patients were recruited, with ACLR with quadruple hamstrings. An intervention group with vancomycin-embedded grafts and the control group without antibiotics. Minimum follow-up of 2 years.
Results: in group A (with vancomycin) of 122 patients, no infections were reported. In group B (without vancomycin) of 123 patients, 3 infections were reported (p = 0.247). In group A, 427 dollars ($3.5 per vial of vancomycin) was spent; while in group B, due to the 3 cases of infection, 4,254 dollars were spent. No differences in relation to surgical time and postoperative pain. Patients in group A recorded greater satisfaction. No significant differences between both groups in relation to functional scores and non-infectious complications such as arthrofibrosis and re-rip.
Conclusions: the study shows that in the context of primary RLCA with STRI grafts, the use of topical vancomycin reduces the incidence of AS and consequently the excessive expenses associated with its treatment; Therefore, it is a valuable, cost-effective strategy. It does not significantly alter functional outcomes, graft healing, or associated non-infectious complications.
Keywords: Septic arthritis; Vancomycin in ACLR; Cost/benefit; Complications
Study Design: II. Prospective Cohort Study
INTRODUCCIÓN
La artritis séptica (AS) ulterior a la cirugía de reconstrucción del ligamento cruzado anterior (RLCA) es una complicación infrecuente, pero potencialmente devastadora. Según diferentes publicaciones, la incidencia de infección puede ser del 0.14 al 1.8 % y típicamente el origen es bacteriano.1 Los patógenos más comunes son el Staphylococcus aureus y los estafilococos coagulasa negativos.2-4 Un tratamiento integral de esta complicación ha demostrado tasas de curación de alrededor del 100 %; sin embargo, los resultados clínicos luego de una AS son peores, incluso a largo plazo.1
Como factores de riesgo generales para el desarrollo de artritis séptica (AS) asociada a RLCA, clásicamente se describe la utilización de injerto de semitendinoso y recto interno (ST-RI), procedimientos abiertos asociados, uso de drenajes y cirugías previas en la misma rodilla.5,6 Dentro de los factores asociados al paciente, el antecedente de diabetes y/o tabaquismo y el sexo masculino han sido reportados también como posibles factores de riesgo de infección.7,8
Desde la utilización de vancomicina como antibiótico tópico para embeber los tendones, se han publicado múltiples trabajos donde se pone de manifiesto la reducción significativa, en aproximadamente 10 veces, de la tasa de infección luego de la RLCA.9-17
Sin embargo, existen pocos estudios que demuestren el costo-beneficio económico que tiene la implementación sistemática de este protocolo en la RLCA. El objetivo principal del siguiente estudio fue evaluar si es costo-efectivo conveniente el uso de vancomicina como coadyuvante para prevenir la AS en la RLCA primaria. En forma secundaria se reportaron resultados funcionales y complicaciones del procedimiento.
MATERIALES Y MÉTODOS
El protocolo del siguiente estudio fue aprobado por el Comité de Ética de la Institución y todos los pacientes firmaron un consentimiento informado aceptando su participación.
Criterios de inclusión y exclusiónSe incluyeron en el estudio pacientes entre 17 y 55 años, con lesión unilateral de LCA, en quienes se realizó una plastia de LCA con injerto de ST-RI cuádruple autólogo. También se consideró como criterio de inclusión una movilidad articular de rodilla con extensión completa y flexión activa mayor a 100°.
Se excluyeron del estudio aquellos pacientes con diagnóstico de diabetes, obesidad (IMC ≥25), tratamientos con inmunosupresores, pacientes con inmunodeficiencias y tabaquistas de más de 20 cigarrillos diarios. También fueron excluidos quienes tenían cirugías previas en rodilla, genu varo artrósico Ahlbäck II en adelante, artrosis femoropatelar o tricompartimental, lesión ligamentaria asociada (LCP, LLI, LLE) de la rodilla, genu varo mayor a 15°, falta de extensión completa y flexión menor a 100°, pacientes con antecedentes de infección y/o radioterapia cercanas a la rodilla y en quienes se realizó una reconstrucción de LCA, transportes osteocondrales y/o trasplantes meniscales en el mismo tiempo quirúrgico. También se excluyeron del estudio aquellos en quienes la plastia del LCA se hizo con otro tipo de injertos (hueso-tendón-hueso, cuadricipital, recto anterior, peroneos, aloinjertos).
Diseño del estudioEstudio prospectivo comparativo y randomizado. Se asignó un paciente a cada tratamiento en forma alternativa. Se estipuló una tasa de asignación de 1:1 para cada grupo.
AleatorizaciónSe utilizó un sistema de aleatorización simple, sobre la base de una secuencia numérica continua, dividiendo grupo de control y grupo de intervención según correspondiera número impar o par. Dicho procedimiento fue llevado a cabo por personal administrativo del sanatorio en el momento de admisión del paciente, se anexó un sobre a la historia clínica del paciente donde se asignaba el uso, o no, de vancomicina tópica en el intraoperatorio. Los cirujanos tomaron conocimiento del grupo al que pertenecía cada paciente en la sala de operaciones, según apertura de dicho sobre por parte de personal de quirófano (instrumentador circulante).
Técnica quirúrgicaEl mismo equipo quirúrgico realizó todas las cirugías y en el mismo quirófano. En todas participaron 2 cirujanos con experiencia en reconstrucción artroscópica del LCA.
En todos los pacientes, se administraron 2 g de cefazolina endovenosa (EV) preoperatoria una hora antes del procedimiento. En casos de alergia conocida a betalactámicos se administró clindamicina endovenosa.
En todos los casos se utilizó manguito hemostático automático en raíz de muslo. En primer lugar se realizó la toma de injerto de ST-RI con incisión medial de aproximadamente 4 cm de longitud y medial a la tuberosidad anterior de la tibia. Además, para todos se preparó el injerto según técnica, con injertos de ST-RI cuádruples, con un diámetro entre 8-9 mm. Una vez preparado el injerto, según numeración del caso (apertura de sobre) se utilizó vancomicina tópica, o no, en el injerto. Todos los injertos fueron sumergidos en 200 cc de solución salina, en los casos que correspondiera se adicionaba y diluía 1 g de vancomicina durante un lapso mínimo de 10 minutos (Fig 1).
En ambos grupos se utilizó la misma técnica quirúrgica, a través del portal anteromedial para emplazar el túnel femoral, intentando replicar una reconstrucción anatómica (Fig 2). Luego de pasar el injerto a través de los túneles, fueron fijados con 2 tornillos interferenciales con rosca roma; tornillos de titanio, de PEEK o de biocompuesto (según provisión por parte de cobertura social del paciente). Al finalizar la artroscopia, se utilizó la solución fisiológica (con vancomicina, o sin esta) para lavar la incisión de toma de injerto. Cierre de herida por planos.
En todos los casos, los pacientes egresaron del quirófano con curación estéril, vendaje elástico e inmovilizador de rodilla. No se utilizaron drenajes.

Figura 1. A) Dilución de 1 g de vancomicina en 200 cc de solución fisiológica. B) Colocación de injertos ST-RI cuádruples durante 10 minutos.
Todos los pacientes fueron rehabilitados con el mismo protocolo, en el centro de rehabilitación del sanatorio en el que se realizó la intervención. Se permitió carga de peso con inmovilizador a partir del día de la cirugía. La inmovilización con férula se mantuvo por 10-15 días. Se iniciaron actividades deportivas sin pivote a partir del sexto mes. Se permitió el regreso deportivo al mismo nivel de exigencia previo a la lesión, a partir del octavo o noveno mes del postoperatorio.
Seguimiento postoperatorioEl dolor en esta etapa se evaluó con una escala visual analógica del dolor (EVA), en la que: ningún dolor = 0, el dolor más intenso imaginable = 10. La definición del nivel de dolor, según EVA, se realizó en el primer control, a las 2 semanas de la cirugía. Esta evaluación se tomó de manera general, tanto a nivel de la rodilla como en el sitio de toma de injerto. Sobre la base de la bibliografía, se consideró 1.4 como diferencia clínicamente significativa.
El nivel de satisfacción del paciente también se registró a través de la escala visual análoga. Se consignó el 0 como el nivel de menor satisfacción y al 10 como el de mayor valor.
La evaluación clínica se basó en la puntuación del IKDC (International Knee Documentation Committee) y Tegner-Lysholm. La determinación de estos scores se efectuó en el preoperatorio (una semana antes de la cirugía) y al momento del alta en el postoperatorio.
Los pacientes fueron seguidos por sus cirujanos a las 2 semanas del postoperatorio, al mes y una vez por mes hasta cumplir el año de la cirugía. Luego del año de la cirugía los controles se realizaron cada 6 meses, con excepciones supeditadas a la aparición de alguna intercurrencia.
Al primer mes del postoperatorio, se realizaron radiografías de frente y de perfil de la rodilla para evaluación de la orientación de los túneles y posición de los elementos de fijación (Fig. 3).
Todos los pacientes fueron evaluados con RNM a los 6 meses para consignar la intensidad de la señal del injerto (Fig. 4).
A los 8 meses de la cirugía, los pacientes fueron evaluados por otro cirujano artroscopista. Los exámenes físicos incluyeron el rango de movimiento, la prueba del cajón anterior, la prueba de Lachman y una de cambio de pivote. Además, se valoró la traslación tibial anterior con el artrómetro de rodilla KT-1000 (MedMetric Corp., CA, EE. UU.). Se analizaron las puntuaciones del International Knee Documentation Committee (IKDC), Tegner-Lysholm para detectar síntomas, nivel de actividad y mejoría funcional.
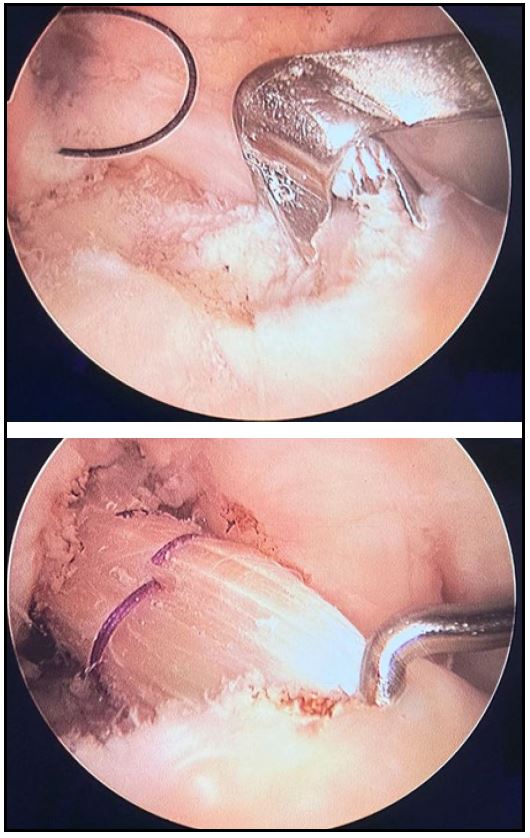
Figura 2. Colocación y fijación de ST-RI cuádruples según técnica anatómica transportal medial con 2 tornillos interferenciales romos.
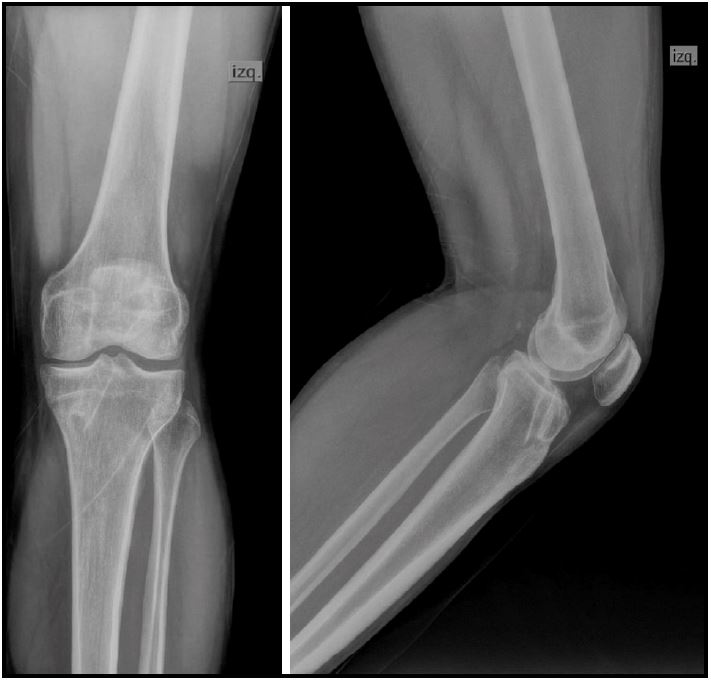
Figura 3. Radiografías de frente y perfil para evaluar la posición de los túneles.
El diagnóstico probable de artritis séptica postoperatoria fue definido como la aparición de síntomas compatibles con infección profunda de la rodilla (derrame articular, pérdida de amplitud de movimiento, edema con supuración, o sin esta), asociado a aumento de reactantes de fase aguda. En todos los casos sospechosos se realizó una artrocentesis con análisis citológico y cultivo. El recuento de células >50000/ml, más de 90 % de neutrófilos y/o un cultivo positivo fueron los criterios diagnósticos de AS que indicaron un tratamiento quirúrgico y antibiótico endovenoso.18
En estos casos se evaluaron los días que transcurrieron desde la cirugía primaria, el número de toilettes realizadas y los microorganismos aislados en los cultivos. En estos casos se registró el costo total de la/s cirugías y del tratamiento antibiótico.
EnmascaramientoLa recolección de datos de los pacientes, la valoración de los scores funcionales y el examen físico al momento del alta médica fueron realizadas por un cirujano artroscopista sin conocimiento del grupo (intervención/control) al que pertenecía cada paciente, actuando como un evaluador ciego.
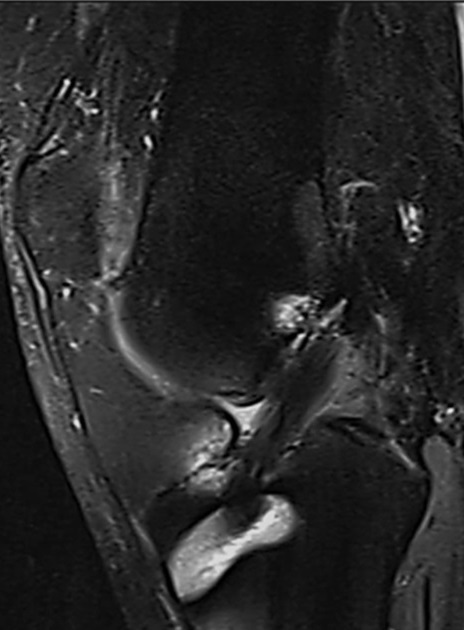
Figura 4. Control con RNM al sexto mes del postoperatorio para evaluar señal del injerto y determinar el grado de madurez.
Entre febrero de 2020 y febrero de 2023 se realizaron 324 RLCA, se excluyeron 12 pacientes a quienes se les adicionó una osteotomía tibial valguizante de apertura medial (OTVAM), 27 en quienes se realizó una revisión de RLCA, 9 a los que se les efectuó transporte osteocondral y 26 casos en los cuales se utilizaron injertos distintos a ST-RI. De esta manera, se reclutaron 250 pacientes, quienes fueron operados de una RLCA con injertos ST-RI cuádruples, sin otro procedimiento asociado. Fueron aleatorizados en 2 grupos: uno conformado por 125 pacientes en quienes se utilizó 1 g de vancomicina (grupo de intervención) disuelta en 200 cc de solución fisiológica y, el otro conformado por 125 pacientes en quienes el injerto STRI fue sumergido en 200 cc de solución fisiológica sin vancomicina (grupo control). Tres pacientes del grupo de intervención (vancomicina) no cumplieron con el seguimiento adecuado, 2 de ellos porque no se pudo consignar seguimiento en tiempo y forma y el otro porque se mudó a otro país. En el grupo de control (sin vancomicina), 2 pacientes no completaron con el seguimiento adecuado (ambos por quedar sin cobertura de salud). Así, el grupo de intervención ST-RI con vancomicina quedó conformado por 122 pacientes y el grupo de control ST-RI sin vancomicina, integrado por 123 pacientes. De esta manera, el número total de la muestra que cumplió con el seguimiento mínimo de 24 meses fue de 245 (Fig. 5).
Cabe destacar que no se realizó un cálculo formal de tamaño muestral, solo se incluyeron aquellos pacientes en esos 3 años (febrero de 2020 a febrero de 2023).
Análisis estadísticoRespecto del grupo de intervención, para analizar las variables categóricas, se emplearon el test de Chi-cuadrado o de Fisher, y para las continuas el test t-Student si se cumplía el supuesto de normalidad y el test de Wilcoxon en caso de que no se verificara dicho supuesto. El supuesto de normalidad de las variables continuas se analizó con el test de Shapiro-Wilk. En todos los test el nivel de significación establecido fue 0.05. Para el procesamiento de los datos se utilizó el programa R.
RESULTADOS
En el apartado “Muestra de pacientes” se detallan las características de la conformación de la muestra (Fig. 5). Las características demográficas en ambos grupos fueron similares (Tabla 1).
En el grupo A (con vancomicina), entre los 122 pacientes no se reportaron infecciones. En el grupo B (sin vancomicina), de 123 pacientes, se reportaron 3 infecciones que requirieron una cirugía de lavado artroscópico sumado a antibioticoterapia endovenosa específica durante un lapso de 2 semanas y luego vía oral (hasta curación infectológica). Si bien la diferencia no fue estadísticamente significativa (p = 0.247), considerando los costos económicos, en el grupo A se gastó el equivalente a un 1 g de vancomicina intraoperatoria (3.5 dólares por ampolla de 1 g) por paciente, con un valor total del grupo de 427 dólares (3.5 multiplicados por 122 pacientes). Mientras que en el grupo B, debido a los 3 casos de infecciones, y a la necesidad de realizar toilette quirúrgica más internación con antibioticoterapia EV y luego por vía oral, se gastaron 4254 dólares en los 3 casos (Tabla 2). En resumen, en el grupo A el costo por paciente fue de 3.5 dólares, mientras que el grupo B (sin vancomicina) este fue de 34.59 dólares; una erogación 10 veces mayor por paciente.
En cuanto al tiempo quirúrgico, entre ambas técnicas no se registraron diferencias estadísticamente significativas. En relación al dolor postoperatorio evaluado con EVA, tampoco hubo diferencias. En lo que respecta al grado de satisfacción del paciente, en lo concerniente al procedimiento quirúrgico, aquellos del grupo A (con vancomicina) registraron mayor satisfacción con diferencias de significación estadística (Tabla 3).
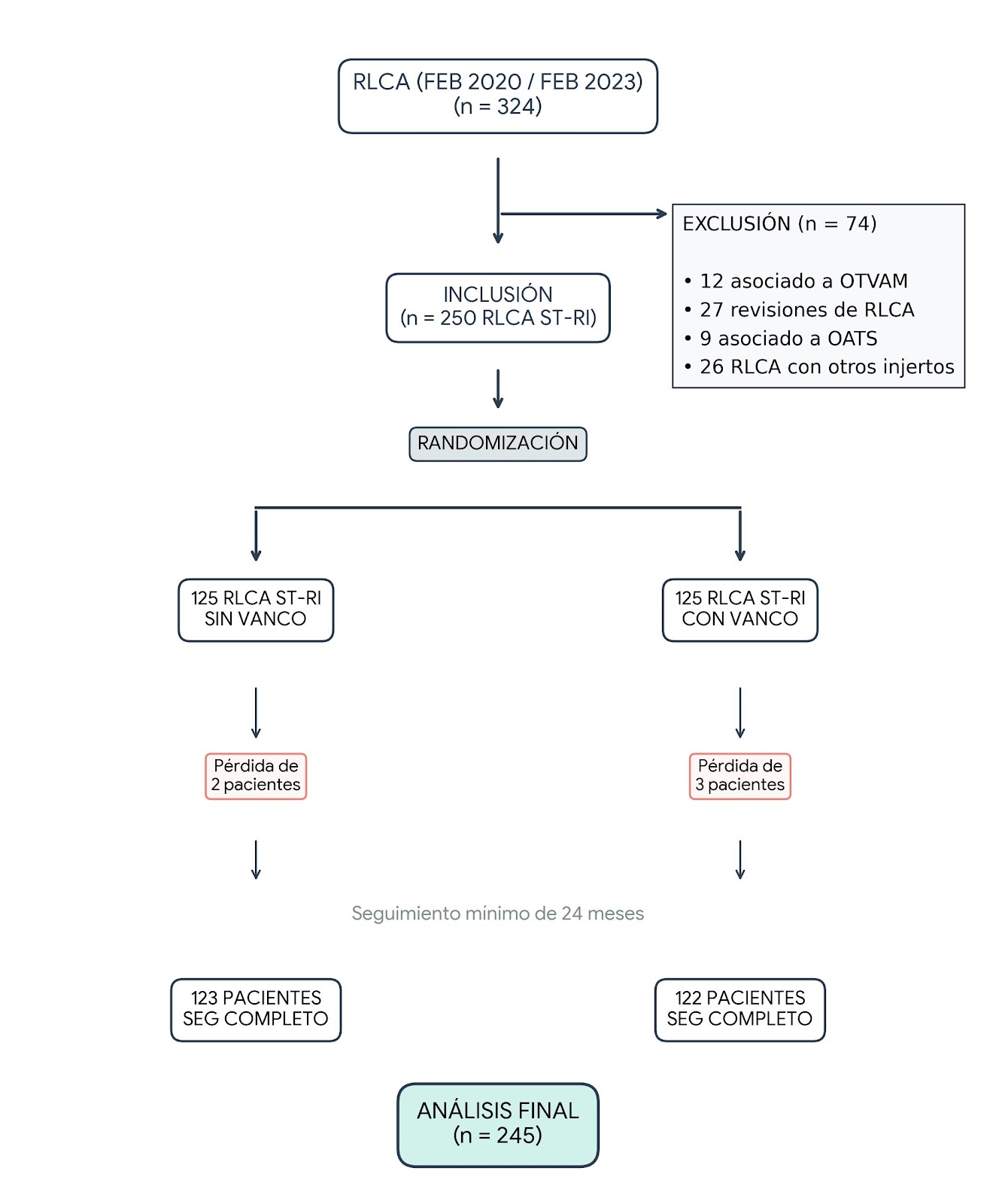
Figura 5. Flujograma de los participantes y su asignación a cada grupo.
| Con vancomicina (n = 122) | Sin vancomicina (n = 123) | Valor p | Total (n = 245) | |
|---|---|---|---|---|
| SEXO | ||||
| F | 34 (28 %) | 37 (30 %) | 0.8100 | 71 (29 %) |
| M | 88 (72 %) | 86 (70 %) | 174 (71 %) | |
| EDAD | ||||
| Mediana [Q1, Q3] | 32.0 [25.3, 38.0] | 34.0 [27.5, 38.0] | 0.209 | 34.0 [27.0, 38.0] |
Q1: primer cuartil. Q3: tercer cuartil. VCO: vancomicina.
| AS con vancomicina (n = 0) | AS sin vancomicina (n = 3) | |
|---|---|---|
| GASTOS QUIRÚRGICOS | ||
| Lavados artroscópicos | 1236 | |
| Estadía en internación | 2503 | |
| Antibióticos EV | 294 | |
| Antibióticos orales | 121 | |
| Consultas ortopédicas | 60 | |
| Consultas infectológicas | 40 | |
| Total | 4254 | |
Montos expresados en dólares. AS: artritis séptica. RLCA: reconstrucción del ligamento cruzado anterior. EV: endovenoso.
No se registraron diferencias estadísticamente significativas entre ambos grupos en relación a los resultados de valoraciones de scores de IKDC, Tegner-Lysholm y valoraciones con el artrómetro KT1000 (Tabla 4).
En los pacientes que habían sufrido una AS se apreció mayor dolor, según la escala EVA en el postoperatorio, una considerable menor satisfacción por el procedimiento realizado y peores resultados de scores funcionales y de artrometría. También, estos pacientes obtuvieron el alta 4 meses más tarde que aquellos que no habían experimentado esta complicación (Tabla 5).
En relación a complicaciones no infecciosas, se registraron 2 casos de artrofibrosis en el grupo A y 1 caso en el grupo B, en los 3 casos se realizó movilización bajo anestesia, con adecuada evolución en todos ellos. En relación a rerroturas del injerto, se constataron 4 casos en grupo A y 5 casos en el grupo B. En ninguno de los casos estas diferencias fueron significativas.
DISCUSIÓN
En virtud de los resultados obtenidos, los principales hallazgos del trabajo fueron:
- En el grupo con vancomicina no se registraron casos de infecciones, en el grupo sin vancomicina sí existieron casos de complicaciones infecciosas; aunque la diferencia no fue estadísticamente significativa.
- El costo de utilizar sistemáticamente vancomicina tópica en el intraoperatorio es menor que el costo asociado al tratamiento de las complicaciones infecciosas; con lo cual se considera un recurso económicamente rentable.
- No se encontraron diferencias significativas entre ambos grupos en relación con los scores funcionales, retorno deportivo y complicaciones no infecciosas asociadas.
- En los casos con complicaciones infecciosas, el dolor postoperatorio fue más intenso, la artrometría tuvo perores resultados y el alta se demoró varios meses.
Luego de la descripción de la técnica de embebido del injerto en vancomicina por Vertullo y cols. en 2012, estos mismos autores publicaron en 2015 la primera serie de 1135 pacientes donde ninguno presentó infección postoperatoria, comparado con una incidencia previa del 1.4 % en 285 pacientes. De forma similar, en una serie de 1640 pacientes, Baron y cols. concluyeron que el uso de injertos impregnados en vancomicina se asoció a una reducción de 10 veces en la infección tras la RLCA (0.1 % frente a 1.2 %; p = 0.032). Además, el IMC y el aumento del tiempo operatorio fueron señalados como factores de riesgo para una infección.1
| Con vancomicina (n = 122) |
Sin vancomicina (n = 123) |
Valor p | Total (n = 245) |
|
|---|---|---|---|---|
| TIEMPO QX | ||||
| Mediana [Q1, Q3] | 65.0 [63.0, 67.0] | 64.0 [62.0, 67.0] | 0.079 | 65.0 [63.0, 67.0] |
| EVA postoperatoria | ||||
| Mediana [Q1, Q3] | 3.00 [3.00, 3.00] | 3.00 [3.00, 4.00] | 0.022 | 3.00 [3.00, 4.00] |
| SATISFACCIÓN | ||||
| Mediana [Q1, Q3] | 9.00 [8.00, 9.00] | 8.00 [7.00, 9.00] | <0.001 | 8.00 [7.00, 9.00] |
Q1: primer cuartil. Q3: tercer cuartil. EVA: escala visual analógica
| Con vancomicina (n = 122) |
Sin vancomicina (n = 123) |
Valor p | Total (n = 245) |
|
|---|---|---|---|---|
| KT-1000 PREOP | ||||
| Mediana [Q1, Q3] | 7.00 [7.00, 8.00] | 7.00 [7.00, 8.00] | 0.993 | 7.00 [7.00, 8.00] |
| KT-1000 POSTOP | ||||
| Mediana [Q1, Q3] | 2.00 [1.00, 2.00] | 2.00 [1.00, 2.00] | 0.008 | 2.00 [1.00, 2.00] |
| IKDC PREOP | ||||
| Mediana [Q1, Q3] | 52.0 [50.0, 52.8] | 52.0 [50.0, 52.5] | 0.916 | 52.0 [50.0, 53.0] |
| IKDC POSTOP | ||||
| Mediana [Q1, Q3] | 84.0 [83.0, 84.0] | 80.0 [79.0, 82.0] | <0.001 | 83.0 [80.0, 84.0] |
| TEGNER-LYSHOLM PREOP | ||||
| Mediana [Q1, Q3] | 55.0 [54.0, 56.0] | 55.0 [54.0, 56.0] | 0.911 | 55.0 [54.0, 56.0] |
| TEGNER-LYSHOLM POSTOP | ||||
| Mediana [Q1, Q3] | 87.0 [86.0, 88.0] | 84.0 [83.0, 86.0] | <0.001 | 86.0 [84.0, 87.0] |
Q1: primer cuartil. Q3: tercer cuartil. VCO: vancomicina
Figueroa y cols. publicaron estrategias para minimizar el riesgo de infección asociada a una RLCA y recomiendan la incorporación de vancomicina tópica a este protocolo. La justificación para el empleo de este fármaco radica en su baja alergenicidad, su estabilidad térmica, la seguridad para su uso local y un gran volumen de distribución. Además, tiene una acción bactericida contra los patógenos más comúnmente aislados en infección luego de una RLCA (Staphylococcus aureus y los estafilococos coagulasa negativos).19
Cuando el injerto es impregnado en vancomicina actúa como un reservorio de antibiótico que se diluirá durante horas sobre la CIM (concentración inhibitoria mínima) de los mencionados microorganismos. También actúa sobre la potencial contaminación que se produce durante la recolección y preparación del injerto.20
| Con AS (n = 3) |
Sin infección (n = 242) | |
|---|---|---|
| SEXO | ||
| F | 0 (0%) | 71 (29%) |
| M | 3 (100%) | 171 (71%) |
| EDAD | ||
| Promedio (DE) | 36.0 (2.00) | 32.3 (7.60) |
| Mediana [Q1, Q3] | 36.0 [35.0, 37.0] | 34.0 [27.0, 38.0] |
| TIEMPO QX | ||
| Promedio (DE) | 64.3 (4.16) | 65.0 (3.42) |
| Mediana [Q1, Q3] | 63.0 [62.0, 66.0] | 65.0 [63.0, 67.0] |
| EVA POSTOP | ||
| Promedio (DE) | 7.33 (0.577) | 3.22 (0.763) |
| Mediana [Q1, Q3] | 7.00 [7.00, 7.50] | 3.00 [3.00, 4.00] |
| SATISFACCIÓN | ||
| Promedio (DE) | 4.67 (0.577) | 8.20 (0.893) |
| Mediana [Q1, Q3] | 5.00 [4.50, 5.00] | 8.00 [8.00, 9.00] |
| KT-1000 PREOP | ||
| Promedio (DE) | 6.67 (0.577) | 7.07 (0.692) |
| Mediana [Q1, Q3] | 7.00 [6.50, 7.00] | 7.00 [7.00, 8.00] |
| KT-1000 POSTOP | ||
| Promedio (DE) | 3.00 (0) | 1.67 (0.573) |
| Mediana [Q1, Q3] | 3.00 [3.00, 3.00] | 2.00 [1.00, 2.00] |
| IKDC PREOP | ||
| Promedio (DE) | 52.3 (1.53) | 51.3 (1.58) |
| Mediana [Q1, Q3] | 52.0 [51.5, 53.0] | 52.0 [50.0, 53.0] |
| IKDC POSTOP | ||
| Promedio (DE) | 75.7 (0.577) | 82.1 (2.24) |
| Mediana [Q1, Q3] | 76.0 [75.5, 76.0] | 83.0 [80.0, 84.0] |
| TEGNER-LYSHOLM PREOP | ||
| Promedio (DE) | 55.3 (1.53) | 55.0 (1.21) |
| Mediana [Q1, Q3] | 55.0 [54.5, 56.0] | 55.0 [54.0, 56.0] |
| TEGNER-LYSHOLM POSTOP | ||
| Promedio (DE) | 77.0 (0) | 85.5 (2.32) |
| Mediana [Q1, Q3] | 77.0 [77.0, 77.0] | 86.0 [84.0, 87.0] |
| ALTA DEPORTIVA | ||
| Promedio (DE) | 12.3 (0.577) | 8.22 (0.759) |
DE: desvío estándar. Q1: primer cuartil. Q3: tercer cuartil.
Park y cols. evaluaron las propiedades biomecánicas de los injertos de ST-RI embebidos en vancomicina, para ello se obtuvieron 10 pares (20 especímenes) de tendones ST-RI cadavéricos humanos frescos congelados. Se prepararon los injertos cuádruples y se aleatorizaron en los grupos de vancomicina y control.
El injerto se expuso a la solución antibiótica durante 15 min (5 mg/ml) y se preparó mezclando 1 g de vancomicina con 200 ml de solución salina normal (NaCl 0.9%). En este estudio in vitro, el prelavado con vancomicina no afectó las propiedades biomecánicas de los tendones, ni su elongación, incluso tras la carga cíclica. El trabajo sugiere que el prelavado con vancomicina podría considerarse una medida preventiva segura y eficaz para las infecciones postoperatorias tras la RLCA.21
Charalambous y cols. evaluaron si el remojo previo del injerto con vancomicina en la RLCA se asocia con un menor riesgo de rerrotura del injerto en comparación con la ausencia de remojo previo con vancomicina; para ello realizaron una revisión sistemática y metaanálisis. Incluyeron 8 estudios, con un total de 907 casos. El trabajo mostró que el riesgo estimado de rerrotura del injerto de ST-RI fue menor en los casos prehumedecidos con vancomicina frente a los que no lo tuvieron (tasa de rerrotura del 3.2 % frente al 6.2 %, razón de riesgos [RR] = 0.507; IC del 95 %, 0.39-0.737; p <0.001). De forma similar, el riesgo estimado de rerrotura del injerto fue menor en los casos prehumedecidos con vancomicina frente a los que no lo tuvieron cuando el análisis incluyó varios tipos de injerto de LCA (tasa de rerrotura del 2.7 % frente al 3.9 %, RR = 0.557; intervalo de confianza [IC] del 95 %, 0.403-0.771; p <0.001). Sobre la base de su análisis, concluyeron que el remojo previo del injerto con vancomicina es una práctica segura y no compromete las tasas de rerrotura del injerto del ligamento cruzado anterior (LCA) ni los resultados clínicos.22
Si bien hay bibliografía que avala el uso de la vancomicina como instrumento para prevenir la AS asociada a RLCA, existe incertidumbre por la probable toxicidad sobre condroblastos y osteoblastos y por el posible impacto negativo sobre las propiedades biomecánicas del injerto. Atherton y cols. evaluaron los efectos moleculares y estructurales de la vancomicina en un injerto ST-RI humano y concluyeron que la vancomicina parece segura y no tiene efectos perjudiciales en la estructura celular o molecular del tendón utilizado para la RLCA.23 En el mismo sentido, Xiao y cols. evaluaron la citotoxicidad de la vancomicina sobre los tenocitos, para ello, aislaron y expandieron in vitro tenocitos patelares humanos. Los tenocitos en cultivo se expusieron a vancomicina en 5 concentraciones diferentes (400, 1600, 3200, 6400 y 12800 μg/ml) y en 3 intervalos de tiempo (2, 6 y 24 horas). Los tenocitos derivados de tendones rotulianos humanos expuestos a concentraciones relativamente altas de vancomicina durante períodos cortos de tiempo no muestran muerte celular ni toxicidad significativas. Con base en esos hallazgos, asumieron que no es probable que la exposición de los tendones a la vancomicina durante un período corto de tiempo, como antes de la RLCA, cause toxicidad en los tenocitos.24
En relación a la maduración/ligamentización del injerto y su visualización a través de imágenes de RNM, Figueroa y cols. realizaron un estudio secuencial retrospectivo de pacientes sometidos a RLCA, comparando un protocolo de injerto sin preinmersión en vancomicina con otro de injerto con preinmersión. Se obtuvieron las puntuaciones de Lysholm y del IKDC tras un seguimiento mínimo de 24 meses. Entre los 6 y los 12 meses de seguimiento se efectuó una resonancia magnética (RNM) para evaluar la consolidación e integración del injerto. Los autores concluyeron que el prelavado con vancomicina de los injertos de isquiotibiales aumentó el número de injertos hiperintensos e isointensos en la RNM. En contraste, se observaron más injertos hipointensos cuando no se utilizó vancomicina, lo que sugiere la presencia de injertos más maduros en ese grupo. Así, el remojo previo con vancomicina de autoinjertos de isquiotibiales en la RLCA se asocia con una mayor señal del injerto en la RNM, aunque sin influir en el resultado clínico.25
Aunque se ha demostrado que remojar previamente los injertos en vancomicina es eficaz en estudios observacionales para la prevención de infecciones en la RLCA, el beneficio económico de la técnica es incierto. En este sentido, Truong y cols. realizaron un estudio de costo-efectividad de la técnica de embeber el autoinjerto con vancomicina y valorar su capacidad en la prevención primaria de infecciones en la RLCA.
Según sus resultados, se observó que la técnica de remojo con vancomicina ofrece un ahorro previsto de 660 dólares (en EE. UU.), 581 dólares australiano (en Australia) y 226 euros (en España) por paciente.
Se observó una mejora de 0.007 años de vida ajustados por calidad en comparación con la profilaxis antibiótica intravenosa sola (4.297 frente a 4.290). Los autores concluyeron que la técnica de prelavado con vancomicina es un método altamente rentable para prevenir la artritis séptica postoperatoria después de una RLCA primaria.26
Dentro de las virtudes del trabajo, su formato prospectivo es un rasgo a resaltar. Que el equipo quirúrgico (personal con experiencia, fundamental para la adecuada manipulación y cuidado de la asepsia del injerto) y el quirófano hayan sido comunes a todos los pacientes también es una fortaleza para la homogeneidad de la técnica utilizada y del ambiente donde se desarrolló el procedimiento quirúrgico. Además, que la valoración funcional de los pacientes haya sido realizada por un médico externo al equipo quirúrgico es un factor valorable. Del mismo modo, que todos los pacientes hayan sido rehabilitados en el mismo centro de rehabilitación contribuye a unificar los protocolos del manejo en el postoperatorio.
Otra fortaleza a resaltar del trabajo radica en que es uno de los pocos estudios que aborda la relación costo/beneficio económico de la utilización sistemática de vancomicina intraoperatoria en la RLCA primaria.
No obstante, este estudio tiene varias limitaciones. En primer lugar, el modelo de aleatorización simple en relación al turno quirúrgico entre número par e impar no es el más recomendable. Además, considerando que la AS es una complicación poco frecuente, el número de casos resulta insuficiente para obtener resultados estadísticamente significativos. En el mismo sentido, podría generar información sustancial adicional la implementación de un modelo de Markov para determinar la relación costo-efectividad y la razón costo-efectividad incremental del prelavado adicional con vancomicina en comparación con el uso aislado profilaxis antibiótica intravenosa.
CONCLUSIÓN
El estudio muestra que, en el contexto de una RLCA primaria con injertos de ST-RI, el uso de vancomicina tópica disminuye la incidencia de AS y, en consecuencia, los gastos excesivos asociados a su tratamiento, por lo que resulta una valiosa estrategia costo-efectiva. No altera en forma significativa los resultados funcionales, la cicatrización del injerto ni las complicaciones no infecciosas asociadas.
REFERENCIAS
- García-Mansilla I, Zuain A, Zícaro JP, Yacuzzi C, Costa-Paz M. Preparación del injerto con vancomicina y su incidencia en la disminución de infección luego de la reconstrucción del LCA. Artrocopia. 2022;29(01): 8-13
- Plante MJ, Li X, Scully G, Brown MA, Busconi BD, DeAngelis NA. Evaluation of sterilization methods following contamination of hamstring autograft during anterior cruciate ligament reconstruction. Knee Surg Sports Traumatol Arthrosc. 2013;21(3):696-701
- Schneider JG, Ormseth B, DiBartola AC, et al. Incidence, common pathogens, and risk factors for infection after primary anterior cruciate ligament reconstruction: a systematic review. J Knee Surg. 2024;37(6):470-481
- Renz N, Madjarevic T, Ferrari M, et al. Recommendations on diagnosis and antimicrobial treatment of infections after anterior cruciate ligament reconstruction (ACL-R) endorsed by ESSKA and EBJIS. J Infect. 2023;86(6):543-551
- Manilov R. Infección en plástica de ligamento cruzado anterior: Factores de riesgo. Artroscopía. 2004;11(2):81-5
- Barker JU, Drakos MC, Maak TG, Warren RF, Williams RJ, Allen AA. Effect of graft selection on the incidence of postoperative infection in anterior cruciate ligament reconstruction. Am J Sports Med. 2010;38(2):281-286
- Novikov DA, Swensen SJ, Buza JA, Gidumal RH, Strauss EJ. The effect of smoking on ACL reconstruction: a systematic review. Phys Sportsmed. 2016;44(4):335-341
- Kraus Schmitz J, Lindgren V, Edman G, Janarv PM, Forssblad M, Stålman A. Risk factors for septic arthritis after anterior cruciate ligament reconstruction: a nationwide analysis of 26,014 ACL reconstructions. Am J Sports Med. 2021;49(7):1769-1776
- Vertullo CJ, Quick M, Jones A, Grayson JE. A surgical technique using presoaked vancomycin hamstring grafts to decrease the risk of infection after anterior cruciate ligament reconstruction. Arthroscopy. 2012;28(3):337-342
- Banios K, Komnos GA, Raoulis V, Bareka M, Chalatsis G, Hantes ME. Soaking of autografts with vancomycin is highly effective on preventing postoperative septic arthritis in patients undergoing ACL reconstruction with hamstrings autografts. Knee Surg Sports Traumatol Arthrosc. 2021;29(3):876-880
- Figueroa D, Figueroa F, Calvo R, Lopez M, Goñi I. Presoaking of hamstring autografts in vancomycin decreases the occurrence of infection following primary anterior cruciate ligament reconstruction. Orthop J Sports Med. 2019 25;7(9):2325967119871038
- Pérez-Prieto D, Portillo ME, Torres-Claramunt R, Pelfort X, Hinarejos P, Monllau JC. Contamination occurs during ACL graft harvesting and manipulation, but it can be easily eradicated. Knee Surg Sports Traumatol Arthrosc. 2018;26(2):558-562
- Pérez-Prieto D, Portillo ME, Torres-Claramunt R, Pelfort X, Hinarejos P, Monllau JC. Contamination occurs during ACL graft harvesting and manipulation, but it can be easily eradicated. Knee Surg Sports Traumatol Arthrosc. 2018;26(2):558-562
- Offerhaus C, Balke M, Hente J, Gehling M, Blendl S, Höher J. Vancomycin pre-soaking of the graft reduces postoperative infection rate without increasing risk of graft failure and arthrofibrosis in ACL reconstruction. Knee Surg Sports Traumatol Arthrosc. 2019;27(9):3014-3021
- Schuster P, Schlumberger M, Mayer P, Eichinger M, Geßlein M, Richter J. Soaking of autografts in vancomycin is highly effective in preventing postoperative septic arthritis after revision anterior cruciate ligament reconstruction. Knee Surg Sports Traumatol Arthrosc. 2020;28(4):1154-1158
- Xiao M, Sherman SL, Safran MR, Abrams GD. Surgeon practice patterns for pre-soaking ACL tendon grafts in vancomycin: a survey of the ACL study group. Knee Surg Sports Traumatol Arthrosc. 2021;29(6):1920-1926
- Kuršumović K, Charalambous CP. Relationship of graft type and vancomycin presoaking to rate of infection in anterior cruciate ligament reconstruction: a meta-analysis of 198 studies with 68,453 grafts. JBJS Rev. 2020;8(7):e1900156
- Ross JJ. Septic arthritis of native joints. Infect Dis Clin North Am. 2017;31(2):203-218
- Figueroa D, Figueroa F, Núñez M, Montes V. Estrategias para minimizar el riesgo de infección posterior a una reconstrucción de ligamento cruzado anterior. Artroscopía. 2021;28(1):92-69
- Pérez-Prieto D, Portillo ME, Torres-ClaraPérez-Prieto D, et al. Contamination occurs during ACL graft harvesting and manipulation, but it can be easily eradicated. Knee Surg Sports Traumatol Arthrosc. 2018;26(2):558-562
- Park HJ, Yoon C, Kang SB, et al. Presoaking hamstring autograft with vancomycin does not jeopardize its biomechanical properties, including graft elongation, after cyclic loading. Knee Surg Sports Traumatol Arthrosc. 2025;33(4):1214-1221
- Charalambous CP, Ahmed EM, Kayali F, Nautiyal H, Kuršumović K, Sutton PM. Vancomycin graft presoaking in anterior cruciate ligament reconstruction surgery is associated with a lower risk of graft rerupture as compared with no vancomycin Presoaking: systematic review and meta-analysis. JBJS Rev. 2023;11(12):e23.00145
- Atherton CM, Spencer SJ, McCall K, et al. Vancomycin wrap for anterior cruciate ligament surgery: molecular insights. Am J Sports Med. 2021;49(2):426-434
- Xiao M, Leonardi EA, Sharpe O, et al. Soaking of autologous tendon grafts in vancomycin before implantation does not lead to tenocyte cytotoxicity. Am J Sports Med. 2020;48(12):3081-3086
- Figueroa F, Figueroa D, Calvo R, et al. Vancomycin presoaking of hamstring autografts in anterior cruciate ligament reconstruction is associated with higher magnetic resonance imaging graft signal without influencing clinical outcome. Arthroscopy. 2022;38(5):1528-1534
- Truong AP, Pérez-Prieto D, Byrnes J, Monllau JC, Vertullo CJ. Vancomycin soaking is highly cost-effective in primary ACLR infection prevention: a cost-effectiveness study. Am J Sports Med. 2022;50(4):922-931