ARTROSCOPIA | VOL. 23, Nº 1 : 15-21 | 2016
Se utilizaron la escala de puntuación VAS y de Karlsson–Peterson.
Se evaluó el grado de satisfacción de los pacientes.
Radiográficamente se midieron ángulos de inclinación talar y cajón anterior, se evaluaron en posiciones de estrés pre y postoperatorio del tobillo.
No hubo perdida de la movilidad articular postoperatoria: la dorsiflexión promedio, medida con un goniómetro, fue de 14,8°, en comparación con 15,1° en el tobillo no operados, y la flexión plantar promedio 46.0°, en comparación con 46.7° en el tobillo no operados.
There was no loss of joint mobility postoperative : The average dorsiflexion measured with goniometer was 14.8°, 15.1° compared to non-operated ankle and plantar flexion average 46.0°, compared with 46.7° ankle unoperated.
Las lesiones ligamentarias del tobillo son los más comunes relacionadas con los deportes. Alrededor del 75% de todas las lesiones de tobillo son esguinces, un 85% de estos son injurias por inversión.1
La mayoría de estas lesiones responderán bien a las medidas conservadoras; sin embargo, a pesar del tratamiento apropiado y la rehabilitación, cerca del 10% al 30% de estos pacientes experimentarán inestabilidad lateral crónica del tobillo (ILCT).1 Además, aunque la rehabilitación a menudo mejora las inestabilidades de tobillo, algunos pacientes eventualmente son candidatos para la reconstrucción quirúrgica de los ligamentos laterales del tobillo debido a la inestabilidad persistente.
Más de 50 procedimientos quirúrgicos se han descrito como tratamiento para la inestabilidad crónica del ligamento lateral del tobillo. Los procedimientos pueden dividirse en reconstrucciones anatómicas y no anatómicas.
En la reconstrucción no anatómica se utiliza el tendón del peroneo lateral corto como en la técnica descripta por Watson-Jones, para recuperar la estabilidad lateral del tobillo. Está generalmente aceptado que el rango de movimiento del tobillo después de una reconstrucción no anatómica está restringido, y que la alteración cinemática de la parte posterior del pie que produce, puede conducir a la artrosis subastragalina.2,3
En la reconstrucción anatómica la posición de las inserciones y el origen de los ligamentos son restaurados, ya sea mediante el uso de tejidos endógenos, injerto sintético o por reparación directa.
La reparación directa consiste en la sutura y conservación del ligamento talofibular anterior (LTFA) y del ligamento calcaneofibular (LCF). Comprende las técnicas de Bostrom, o la Bostrom modificada por Gould, y la técnica de Karlsson.4
Las reconstrucciones se basan en el uso de autoinjertos o aloinjertos.5
Sin embargo, la mejor opción quirúrgica sigue siendo discutible.
Las tasas de éxito después de la reparación anatómica han sido tan altas como el 96%. Sin embargo, un subconjunto de la población puede experimentar discapacidad crónica. Algunos autores han postulado que las lesiones intrarticulares son las encargadas de estos síntomas crónicos.6,7 La causa del dolor persistente de tobillo después de la reconstrucción de los ligamentos no ha sido totalmente determinada. La incidencia de las lesiones condrales se ha observado que van de 25% a 95%. Se presume que las lesiones condrales, la sinovitis, los osteofitos anteriores de la tibia o el astrágalo son la causa del dolor persistente de tobillo después de la reconstrucción ligamentaria exitosa.
El tratamiento artroscópico de las lesiones intrarticulares, junto con la reconstrucción anatómica ligamentaria lateral del tobillo, tiene buenos resultados funcionales a mediano plazo.
MATERIALES Y MÉTODOS
Evaluamos en forma retrospectiva 20 tobillos (20 pacientes) con inestabilidad crónica a los que se le realizó un tratamiento combinado de estabilización lateral anatómica un tratamiento artroscópico de las lesiones intrarticulares, desde el año 2010 a 2014.
Los criterios de inclusión para el procedimiento quirúrgico fueron el dolor asociado a inestabilidad lateral del tobillo resultado de esguinces repetitivos en inversión, de por lo menos 6 meses de duración. Los pacientes fueron considerados para la cirugía si el tratamiento conservador, incluyendo terapia física, inmovilización y medicamentos antiinflamatorios, no pudieron mejorar los síntomas. Y si presentaban evidencia de inestabilidad lateral del tobillo por exámenes clínicos de estrés en varo y prueba del cajón anterior positivos.
Se solicitaron radiografías de tobillo frente y perfil con stress en varo y cajón anterior.
Fueron considerados para la reconstrucción ligamentaria los exámenes radiográficos que mostraron: talar tilt mayor a 10, y traslación anterior del astrágalo usando el test de cajón anterior.
Se solicito resonancia magnética nuclear (RMN) preoperatoria de tobillo en todos los casos.
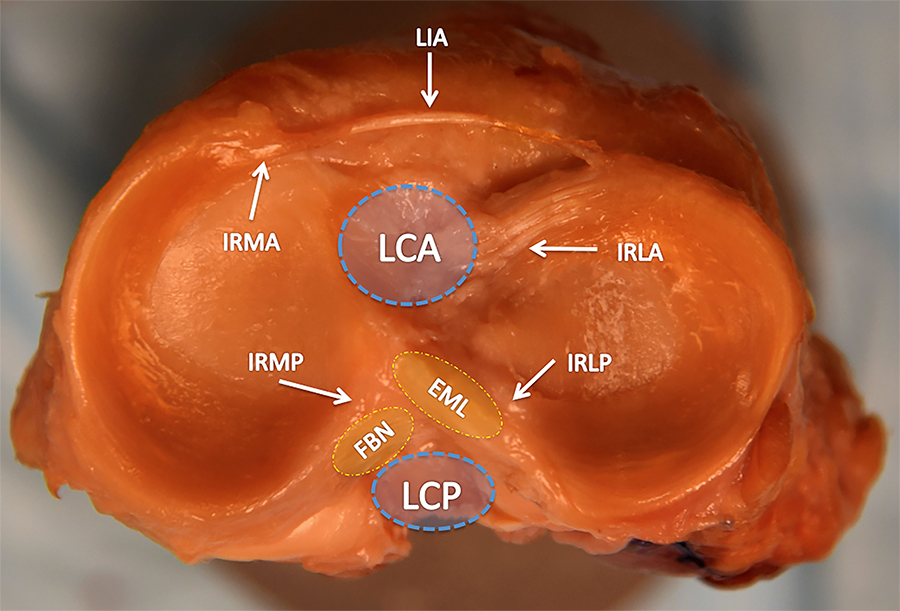
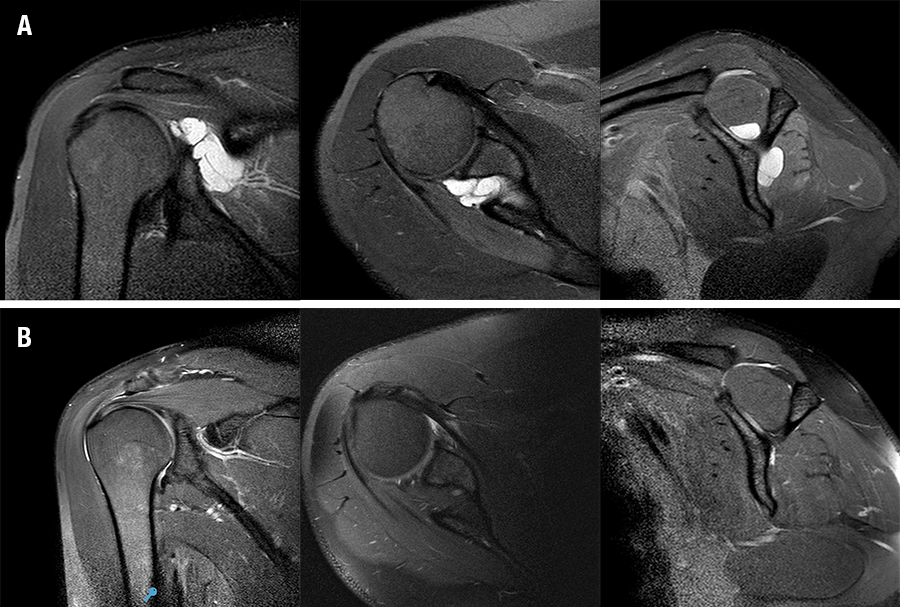
Para visualizar lesiones condrales u osteocondrales del astrágalo, sinovitis, impigment anterolateral u ostefito anterior de la tibia distal y cuerpos libres. Y evaluar la condición de los ligamentos LTFA y LCF (fig. 1).
Los 20 pacientes fueron evaluados con un seguimiento promedio de 25 meses postoperatorio. Para su evaluación se utilizó la escala de puntuación de VAS y de Karlsson-Peterson pre y postoperatoria.
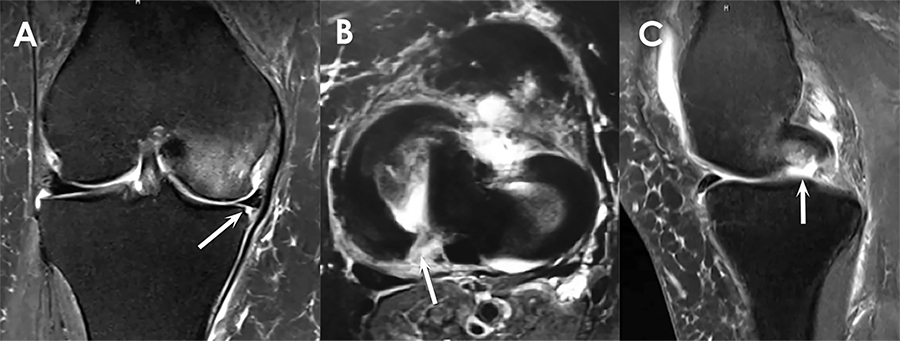
Los pacientes fueron físicamente examinados antes de la cirugía y en el último control postoperatorio. Se evaluó la movilidad de los tobillos (dorsiflexión y flexión plantar) y subtalar (inversión y eversión). Se midió el rango de movimiento subtalar en la posición prona con rodilla flexionada a 90 grados utilizando un goniómetro estándar. Para el análisis radiográfico final de seguimiento, se determinaron ángulos de varo, estrés y cajón anterior talar (distancia entre el margen antero-inferior de la tibia distal y la extremo anterosuperior de la cabeza del astrágalo) fueron medidos y comparados con datos preoperatorios (fig. 2).
Figura 1: A- Lesión ligamentaria lateral del tobillo, B- Lesión osteocondral medial del astrágalo.
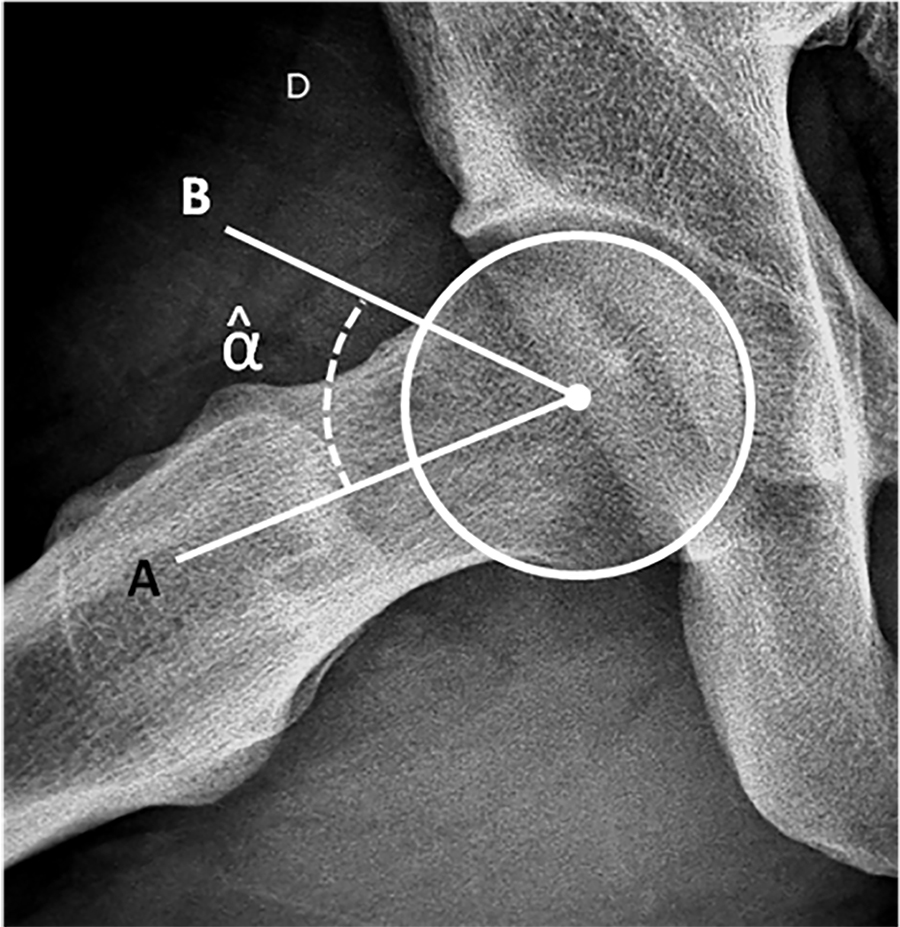
Figura 2: Evaluación radiológica: A- Tilt test y medición de la inclinación talar. B- Cajón anterior y medición radiográfica.
TÉCNICA QUIRÚRGICA
La cirugía fue realizada bajo anestesia espinal. Los pacientes fueron colocados en la posición supina. Se aplicó un torniquete en el muslo. Primero se realizó un procedimiento artroscópico de tobillo. Se utilizó tracción del tobillo no invasiva. Con artroscopio de 3,5 mm y 30°. Se utilizaron los portales anteromedial y anterolateral estándar para examinar la articulación del tobillo.
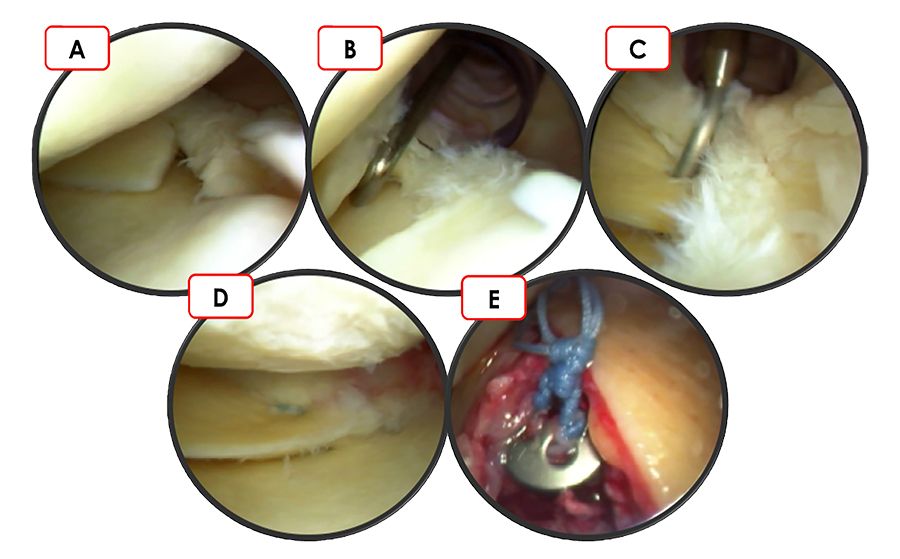
Durante la artroscopía se clasificaron y se trataron las lesiones ostecondrales y se registraron la presencia de osteofitos distales de la tibia q y síndromes de fricción lateral. Se realizó la estabilización lateral: reconstrucción anatómica percutánea de los ligamentos laterales del tobillo, después del procedimiento artroscópico (fig. 3).
Se obtuvo un injerto de semitendinoso de la pierna ipsilateral. El injerto debe tener al menos 9 cm de longitud; siendo en promedio de 3,5 cm del largo destinado para el LTFA y 4,5 cm para el LCF. Se colocaron puntos de tracción tipo Krakow en ambos extremos. Se realizó un túnel oblicuo de posterior a anterior, y de distal a proximal en el maléolo peroneo. Se realizaron 2 incisiones de 1cm una anterior y otra posterior al extremo distal del peroné, se coloco un clavija guía en la región posterior del peroné bajo control radioscópico, se creó un túnel 5 mm oblicuo en el peroné entre 7 y 13 mm proximal a la punta del peroné, perforado en dirección de posterior a anterior y de inferior a superior. Se utilizó una freza de 5 mm canulada para crear los túneles en el astrágalo, peroné y el calcáneo. El diámetro de los túneles óseos debe estar comprendido entre 0,5 y 1,0 mm mayor que el tamaño del tendón.
Se pasó el injerto a través del túnel en el maléolo peroneo con aguja pasatendón de posterior a anterior (fig. 4).
Figura 3: Visión artroscópica de la articulación tibio-astragalina. A- Ostefito distal de la tibia, B- Resección con burr de osteofito tibial, C- Lesión osteocondral grado IV (flecha), D- Realización de microperforaciones en lesiones osteocondrales grado IV.
Figura 4: A- Tunelización del peroné, B- Pasaje del injerto, C- Fijación en el borde posterior con arpón. Se fijó el injerto, con un arpón de titanio de 2.9 mm con sutura reforzada, colocado en el borde posterior del peroné junto a la salida del orificio del túnel.
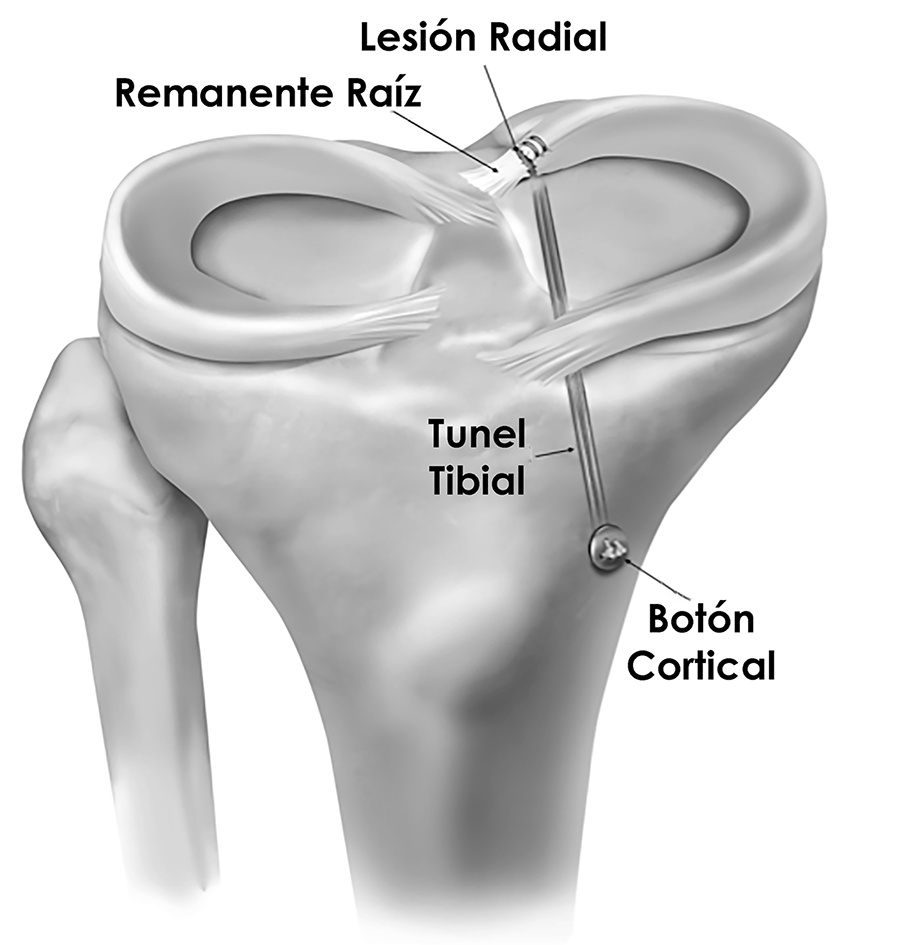
Esto permitirá la tensión individual de cada ligamento: LTFA y LCF. Posteriormente se realizó un túnel en el calcáneo: Se hizo una incisión de 1 cm para exponer el tubérculo del calcáneo. Una clavija guía se coloco bajo control radioscópico en el tubérculo del calcáneo y atravesó desde el aspecto lateral al medial. A través de esta clavija guía se frezo un túnel de 5 mm de diámetro y de 30 mm de longitud. Se realizó el tensado del injerto LTFA y la fijación con el tobillo en leve eversión. Para la fijación en el calcáneo se coloco un tornillo de interferencia biodegradable de 7 x 25 mm, asegurando que el talón permanezca en leve eversión y el tobillo en posición neutra. Por último, se realizó el túnel en el astrágalo: se colocó una clavija guía distal al borde del cartílago del astrágalo y 20 mm proximal a la articulación subastragalina, siempre bajo control radioscópico, se realizó un túnel de 25 mm de profundidad con freza de 5 mm (fig. 5).
Cuando lo permitió la longitud del injerto se utilizó el tendón del semitendinoso en forma doble. Se introdujo el extremo del injerto que corresponderá al ligamento peroneoastragalino con aguja pasa tendón desde lateral a medial en el astrágalo. Se realizaron varias veces movimientos del tobillo de rango completo para confirmar la isometricidad y ajustar la tensión del injerto.
Se fijó en el astrágalo con tornillo de interferencia biodegradable de 6 x 25 mm. La cápsula se suturó para cubrir el injerto, y se cerraron las incisiones (fig. 6).
Después de la operación, el tobillo fue inmovilizado en una posición neutra con una bota plástica por 21 días. Ejercicios de rehabilitación incluyendo contracción isométrica de grupos musculares alrededor de la articulación del tobillo se iniciaron desde el día después de la cirugía. Al mes de la cirugía se indicó movilidad activa. Deambulación con muletas con descarga parcial durante los primeros 15 días. No se permitió una actividad intensa y deportes de contacto hasta 6 meses después de la cirugía.
Figura 5: Ubicación del túnel astragalino, bajo control radioscópico.
Figura 6: Fijación en el calcalcaneo y en el astrágalo con tornillos de interferencia biodegradable. Final de la técnica percutánea.
RESULTADOS
La edad promedio de los pacientes fue de 25 años, rango de 19 a 39.
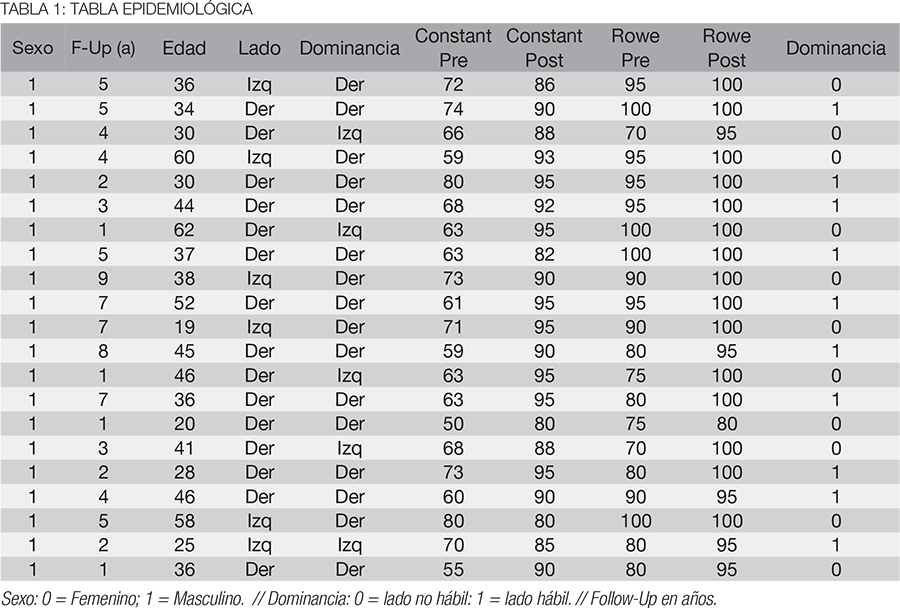
En la escala de puntuación de Karlsson–Peterson preoperatoria la puntuación fue 38,5 puntos, y esto aumentó significativamente a 80,75 puntos final. Los rangos de movimiento subtalar no fueron significativamente diferentes, pero ningún tobillo demostró una limitación significativa tibioastragalina o del rango de movimiento subastragalino postoperatorio. A todos los tobillos se les realizó exploración artroscópica: 12% de los tobillos tenían una lesión osteocondral del astrágalo grado I-II y se las trato con desbridamiento, el 25% tenían una lesión osteocondral grado III-IV y se las trato con autoinjerto osteocondral o microfracturas. Se encontró sinovitis marcada en 10 tobillos y fueron tratados con sinovectomía artroscópica. Ocho de los tobillos presentaba un osteofito distal de la tibia, en los cuales se realizó la resección del osteofito, 4 tobillos presentaban impigment anterolateral. Tres casos tenían lesión osteocondral grado I-II y fueron tratados con desbridamiento, y 5 presentaban lesión osteocondral grado III_IV y se les realizó microfracturas o mosaicoplastia (tabla 1).
Se comparó la movilidad postoperatoria al final del seguimiento con la movilidad del tobillo contralateral. En los 20 pacientes con reconstrucción de ligamentos del tobillo la dorsiflexión promedio, medida con un goniómetro, fue de 14,8°, en comparación con 15,1°en el tobillo contralateral, y la flexión plantar promedio 46.0°, en comparación con 4677° en el tobillo no operados. El movimiento promedio retropié fue de 20,2°, en comparación con 19,8° en el tobillo no operado (tabla 2).
Mientras que en la evaluación radiográfica se obtuvieron los siguientes resultados: disminuyó la inclinación talar de 11,5 a 3,5 y la prueba de cajón anterior disminuyó de 7 mm preoperatoria a 3 mm postoperatoria (tabla 3).
En cuanto a las complicaciones postoperatorias: 1 paciente presento inestabilidad persistente, 1 paciente se quejó de la neuralgia del nervio sural en el postoperatorio, que resolvió después del tratamiento conservador.
DISCUSIÓN
Entre 20% a 40% por ciento de los esguinces de tobillo causan inestabilidad crónica del mismo y la reconstrucción quirúrgica de los ligamentos laterales está indicada cuando la terapia de rehabilitación no lo logra. Muchos son los artículos que se han presentado con las técnicas quirúrgicas para el tratamiento de la inestabilidad lateral crónica de tobillo.
Nuestro estudio demuestra que la técnica descripta, que implica la reconstrucción anatómica del ligamento LTFA y del LCF, utilizando autoinjerto de tendón del semitendinoso y tornillos de interferencia y arpón para su fijación, es una opción viable para el tratamiento de la inestabilidad lateral crónica del tobillo con fijación estable del tendón y proporcionando resultados clínicos satisfactorios.
Las cirugías reconstructivas para inestabilidad lateral del tobillo pueden ser clasificadas como anatómica o no anatómica.
La técnica anatómica incluyen la reparación de los ligamentos laterales tipo Bostron-Gould y la reconstrucción de los ligamentos laterales con un injerto autólogo, aloinjerto o sintético.
Las técnicas no anatómicas consisten en tenodesis que utilizan el tendón del peroneo lateral corto: como la Watson-Jones, Evans y Chrisman-Snook.
El tendón del peroneo lateral corto es el principal estabilizador dinámico de la parte lateral del tobillo. Los procedimientos de tenodesis también son invasivos en términos de abordaje y además tienden a restringir la movilidad del tobillo excesivamente en comparación con procedimientos de reconstrucción anatómica; a su vez en pacientes sometidos a reconstrucciones no anatómicas se informó durante el seguimiento a largo plazo, inestabilidad subjetiva, cinemática no fisiológica y cambios degenerativos del tobillo.4,8
Un estudio de Krips y Niek van Dijk,9 que compara los resultados en atletas a los que se le realizó reparación no anatómica (tenodesis), con aquellos a los que se le realizó una reparación anatómica, mostró mejores resultados con la técnica anatómica. A los pacientes que se les realizó tenodesis tenían limitación mayor de la dorsiflexión del tobillo. En los controles radiográficos postquirúrgicos a los pacientes que se les realizó la técnica no anatómica tenían más osteofitos mediales, y en las radiografías con stress mayor laxitud.
Para lograr una reconstrucción anatómica y estable del ATFL y del CFL, la reconstrucción de los ligamentos laterales utilizando autoinjerto se ha vuelto popular.
Aunque se han introducido algunas técnicas que utilizan un injerto sintético (de fibra de carbono), o un aloinjerto como ligamento.10
En algunos estudios que utilizan un injerto tendinoso y la fijación con arpón y sutura al hueso, han demostrado ser biomecánicamente más débil que la fijación con tornillo de interferencia.
Un trabajo biomecánico realizado por Waldrop, que compara la reparación del ligamento LTFA fijándolo al maléolo peroneo con arpones y suturas, mostró que esta tiene la misma resistencia que la reparación con sutura tipo Bostrom, y una debilidad del 50% comparada con el ligamento intacto.11
Durante el período de evaluación, cuando utilizamos tornillos biodegradables, no se observo ningún tipo de aflojamiento después de la fijación estable.
En concordancia con nuestros resultados Schmidt et al.12 informaron que la cirugía reconstructiva anatómica en casos de inestabilidad lateral del tobillo, no causó ninguna restricción de la amplitud de movimiento en la tibioastragalina ni en la subastragalina y la indican para mantener resultados clínicos satisfactorios a largo plazo.
También consideramos que un injerto de semitendinoso doble de 6 mm de diámetro es lo ideal como injerto.
Nuestros resultados en cuanto a la movilidad postoperatoria de la articulación del tobillo y del retropié son muy buenos, y coinciden con los mostrados por otros estudios en los cuales se realizó una reconstrucción anatómica con injerto de semitendinoso, como el de Yinghui Hua que utiliza un aloinjerto de semitendinoso.13
La técnica percutánea que nosotros describimos en este trabajo es una técnica segura y reproducible, que disminuye los riesgos de lesiones nerviosas y tendinosas, así como las complicaciones asociadas a la herida, al evitar grandes incisiones.
Otro tema es la utilidad de la artroscopía en el tratamiento simultáneo de la inestabilidad lateral crónica del tobillo. Esta tiene un papel primordial por que permite la evaluación y tratamiento de lesiones comúnmente asociadas que afectan el pronóstico después de la reparación ligamentaria.10 Permite la evaluación de la integridad de los ligamento (ATFL, CFL), contribuyendo así al cirujano a decidir qué técnica de reparación es más apropiado para cada caso.2
Pacientes sometidos a estabilización lateral del tobillo, frecuentemente tienen asociadas lesiones intrarticulares: sinovitis, lesiones osteocondrales, osteofitos anterior de la tibia y síndromes de fricción anterolateral, que pueden conducir a dolor persistente si no se tratan, y ser una fuente de dolor residual si no se abordan. Cierta controversia existe si las lesiones intrarticulares debe tratarse en el mismo acto que se realiza la estabilización lateral tobillo o si los procedimientos deben ser tratados en forma separada. Las preocupaciones incluyen la extravasación del líquido de la artroscopía en la zona, que conduzca a alguna dificultad durante la etapa abierta de la cirugía, diferentes programas de rehabilitación y la duración de la operación. Nuestros resultados a mediano plazo del tratamiento concomitante de las lesiones osteocondrales y la inestabilidad crónica del tobillo lateral muestran que se trata de una opción quirúrgica viable.5
Según Okuda,14 la inestabilidad lateral crónica del tobillo se asocia en un 63% con lesiones condrales, especialmente en la parte medial del astrágalo, independientemente del grado de inestabilidad del tobillo, edad y género. La presencia de una lesión osteocondral tiene un efecto negativo en el resultado global en los pacientes que se someten a la estabilización del tobillo como un procedimiento aislado. Por lo tanto, el tratamiento simultaneo artroscópico de una lesión osteocondral y la estabilización lateral abierta del tobillo es el procedimiento recomendado.14
Nuestro trabajo también coincide con el de Choi, respecto a la asociación de las lesiones intrarticulares con las inestabilidades laterales crónicas de tobillo. En la artroscopía que realizó previa a la reconstrucción ligamentaria con la técnica de Bostrom modificada encontró un 96,9% de lesiones intrarticulares, 81,5% de sinovitis anterior, impigment anterolateral en el 38,5 % y lesión osteocondral del astrágalo en el 23,1% de los casos;15 y se refiere a la importancia del tratamiento de estas para mejorar el resultado clínico de la reparación ligamentaria.
Según Gregush,16 la artroscopía tiene un papel primordial en el tratamiento simultáneo de la inestabilidad crónica del tobillo por que permite la evaluación y tratamiento de lesiones comúnmente asociadas que impactan en el resultado después de la reparación del ligamento y confirma la integridad de los ligamentos (ATFL, CFL), así ayuda al cirujano a decidir qué técnica de reparación es más apropiado.17
La importancia del trabajo es la descripción de una técnica quirúrgica percutánea y artroscópica que logra el posicionamiento anatómico y la fijación estable. La debilidad es que los resultados se basaron en un número relativamente pequeño de casos y el periodo de seguimiento fue relativamente corto. Así, el estudio a gran escala adicional es necesario con un seguimiento a largo plazo.
CONCLUSIONES
La reconstrucción percutánea y anatómica del LTFA y LCF usando como autoinjerto el tendón de semitendinoso y la fijación firme con tornillos de interferencia y arpón, puede ser realizada como una alternativa viable para el tratamiento de la inestabilidad lateral crónica del tobillo, especialmente para los tobillos con tejidos ligamentarios laterales pobres.
El método percutáneo disminuye los riesgos y complicaciones de los abordajes extensos, es mejor estéticamente y acorta los tiempos quirúrgicos.
El tratamiento artroscópico de las lesiones intrarticulares junto a la estabilización lateral del tobillo mejoran los signos y síntomas clínicos, favoreciendo los resultados en el mediano plazo.